Leggi di Gay-Lussac e Boyle
Prima legge di Gay-Lussac: dilatazione volumica di un gas a pressione costante
La prima legge di Gay-Lussac non descrive soltanto il riscaldamento di un gas, ma anche il suo raffreddamento:
- un gas riscaldato a pressione costante si dilata (il suo volume aumenta);
- un gas raffreddato a pressione costante si contrae (il suo volume diminuisce).
Possiamo semplificare la formula della prima legge di Gay-Lussac in:
Il volume occupato da un gas mantenuto a pressione costante è direttamente proporzionale alla sua temperatura assoluta.
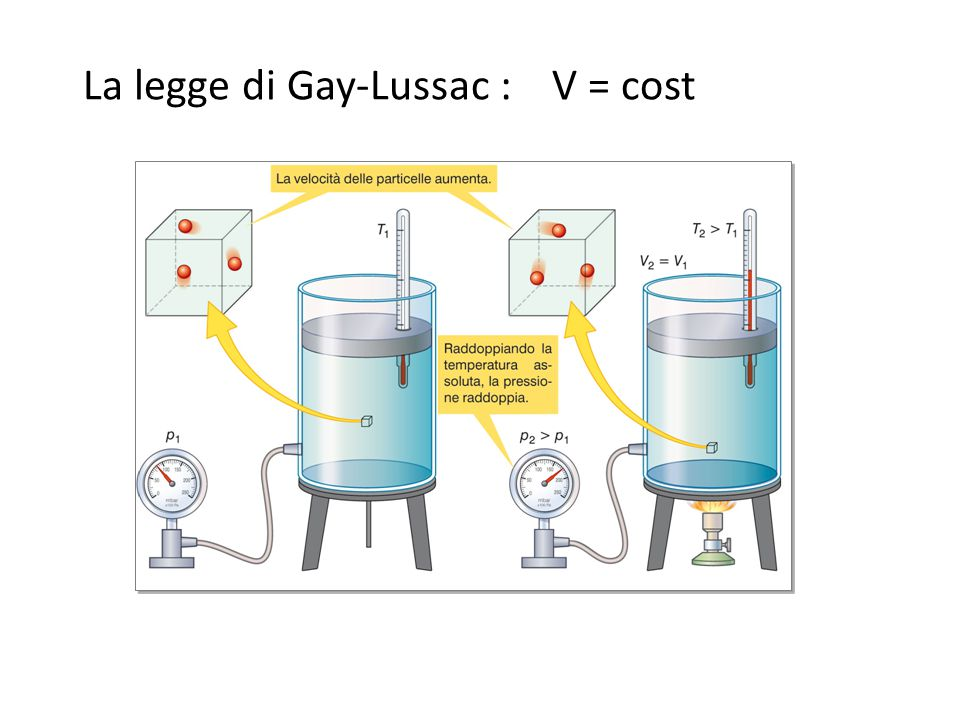
Seconda legge di Gay-Lussac: pressione e temperatura di un gas a volume costante
La legge sperimentale che descrive l'aumento di pressione del gas quando cambia la sua temperatura a volume costante è la seconda legge di Gay-Lussac:
A volume costante la pressione di un gas è direttamente proporzionale alla sua temperatura assoluta
La legge di Boyle: pressione e volume di un gas a temperatura costante
La legge di Boyle stabilisce che, a temperatura costante, il prodotto del volume occupato da un gas per la sua pressione rimane costanteTutto ciò è espresso nella seguente equazione:
Il gas perfetto
Un gas ideale che obbedisce esattamente alle due leggi di Gay-Lussac e alla legge di Boyle si chiama gas perfettoLe tre leggi sperimentali possono essere sintetizzate in un'unica relazione chiamata " equazione di stato del gas perfetto"
Il prodotto della pressione di un gas perfetto per il volume che esso occupa è direttamente proporzionale alla sua temperatura assoluta
-Angela Serra -Giorgia Matassa